研究内容
私たちのグループは、脳が比較的コンパクトであり(0.5mm程度)、高度な遺伝子改変技術を用いることができるショウジョウバエをモデルに、特に翻訳制御という観点から脳機能の解明を目指しています。
なぜハエなのか
ショウジョウバエは、脳を構成する10万以上の神経細胞が形成するシナプス構造・神経ネットワークが電子顕微鏡レベルで記載されている、極めて優れた神経科学のモデル動物です。特定の匂いを砂糖報酬や電気ショック罰と結びつけて学習する連合学習や、繰り返し飲酒によってアルコールの摂取量が日ごとに増加するアルコール依存モデル、メスに拒絶されて求愛行動が抑制される求愛学習など、様々な経験依存的な行動が知られています。また、何十万種類ものトランスジェニック系統や変異体を世界中のストックセンターからクリック一つで入手することができ、ほぼ全ての遺伝子の機能を解析するためのツールが揃っています。「脳はどのように機能し、変化するか」という根源的な問いに対して基盤的なアプローチができるモデル系といえます。
なぜ翻訳を解析したいのか
行動を制御する神経ネットワークの構築や、その可塑的変化には、ゲノムにコードされた遺伝子の発現が極めて精緻に制御されることが必要不可欠です。これまで、遺伝子の転写産物を定量するトランスクリプトーム解析が広く行われ、細胞種や外界刺激に特異的な転写制御の解明が進んできました。ところが最近の研究により、翻訳段階での制御も神経機能に極めて重要な役割を果たすことが明らかになっています。FMR1, mTOR経路、eIF2alphaのリン酸化酵素など、様々な翻訳調節因子の破綻が知的発達症、自閉症、ADHDなど神経機能疾患の発症と関連づけられています。また、mRNA量だけでは細胞内タンパク質の量の30-40%程度しか説明できず、単一mRNAでも複数の翻訳開始部位が使われたり、一部の終止コドンが読み飛ばされて長いタンパク質が翻訳されるストップコドンリードスルーなど、質的にも量的にも翻訳の段階でタンパク質合成が調節されていることが明らかになりつつあります。神経系におけるタンパク質翻訳制御は、今後の重要なフロンティアの一つといえます。
以上をふまえ、私たちはハエの行動測定や神経の構造観察技術と、タンパク質翻訳の解析技術を組み合わせて研究を進めています。
行動解析、遺伝学、解剖学
匂いと電気ショックを連合した嗅覚罰学習、砂糖報酬を連合した嗅覚報酬学習を高精度かつハイスループットでテストする実験系を立ち上げました(図1)。また、アルコール・覚醒剤・毒物などを含んだ餌の摂取をナノリットル単位で測定し、薬物嗜好性の変化を長期間にわたって測定することができます(図2)。トランスジェニック技術やゲノム改変を通して特定の神経や分子を脳内で蛍光ラベルし、その脳内分布を可視化します(図3)
ゲノムワイドな翻訳解析
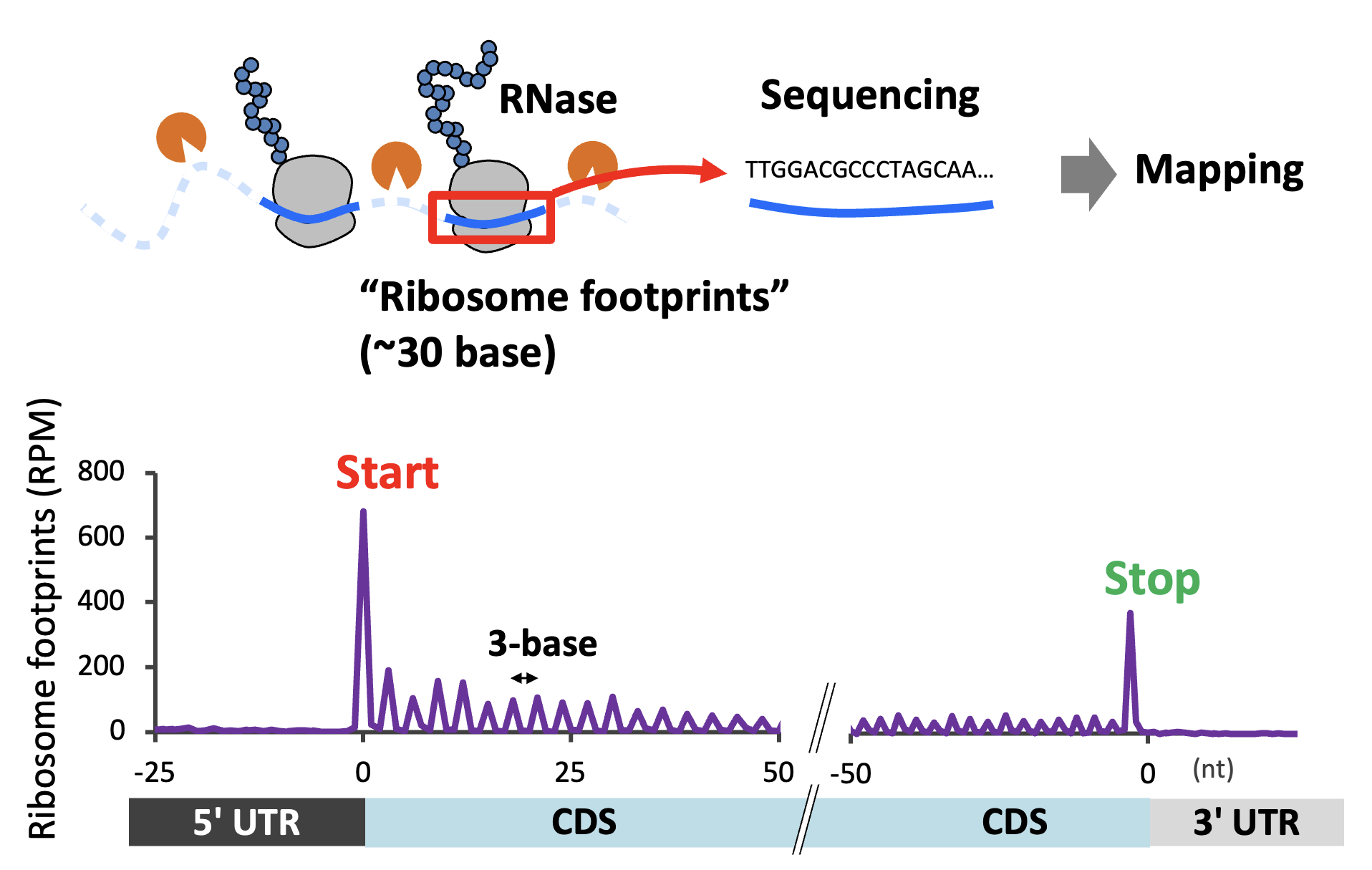
リボソームプロファイリング法は、mRNA上のリボソームの位置を網羅的に決定することで翻訳を解析する技術です。私たちはハエのトランスジェニック標識とリボソームプロファイリング法を組み合わせ、脳の標的細胞から特異的に翻訳を解析する実験を行なっています(図4)。
学習、薬物や毒物の摂取、特定の神経活動によってタンパク質翻訳はどう変化し、どう行動に寄与するか?また、神経系におけるストップコドンリードスルーやuORFの翻訳など非典型的な翻訳はどういった意味をもつのか?といったトピックについて研究を進めています。